1.10 Термодинамиканың бірінші заңы
|
|
|
«ТЕРМОДИНАМИКАНЫҢ БІРІНШІ ЗАҢЫ- энергияның сақталу және түрлену заңын сипаттап, жылудың жұмысқа, жұмыстың жылуға айналуы мүмкін екендігін дәлелдейді»
Термодинамиканың бірінші заңы жалпы жағдайда энергияның сақталу және өзгеру заңын бейнелейді. Бұл заң барлық процесстерге мындай шарттар қояды:
1. Энергия жоқтан пайда болмайды және жоғалмайды, ол бір түрден екінші түрге өзгереді. Механикалық энергияның жылуға айналуы былай өрнектеледі
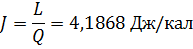
J жұмыстың термиялық эквиваленті. A жылудың механикалықэквиваленті
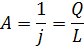
2. Энергия жұмсамай пайдалы жұмыс алатын бірінші текті мәңгілік двигатель құру мүмкін емес.
3. Толық тұйықталған жүйенің ішкі энергиясы тұрақты шама болып табылады. Бұл тұжырымның дұрыстығын төмендегі өрнектер дәлелдейді.Термодинамиканың бірінші заңын жазу үшін, денеге қандай да бір Q жылу берілген. Осы жылу ішкі энергияның өзгерісіне және атқарылатын жұмысқа кетеді. Онда m массалы дене үшін эквиваленттік теңдеу былай
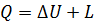 (1.18)
(1.18)
Мұндағы Q = mq; ∆ U = m ∆ u; L = ml
Шексіз аз процесс үшін
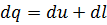 (1.19)
(1.19)
(1.19) теңдеуіне толық тұйықтау шартын қолданамыз, яғни dQ = 0, dl = 0 (жүйе сыртқы ортамен жылу алмаспайды және жұмыс жасамайды). Онда du =0 немесе u = const . Тұйықталған жүйеде қандай процесс жүрсе де, оның ішкі энергиясы тұрақты болып қалады. Жұмыстың өрнегін негізгі күй параметрлері арқылы табамыз (сурет 5).
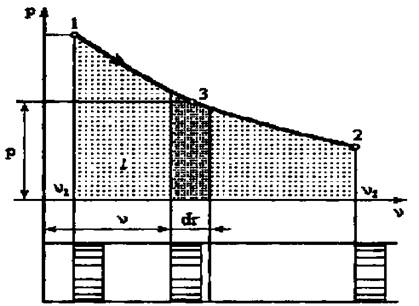
сурет 5. Поршеньдік цилиндрдегі газдың сығылу мен ұлғаю жұмыстарын анықтауға арналған диаграмма
1 кг газдың жұмысы поршеньді шексіз аз оңға жылжытқанда dl = pSdr тең. Мұндағы P қысым 3 - нүктесіндегі қысым, S поршеннің көлденең қимасының ауданы, r поршеннің жылжуы. Sdr = dv болғандықтан,
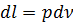 (1.20)
(1.20)
1-2 процестің барлық жұмысы v 1 132 v 2 v 1 ауданына тең. Жұмыстың айқын өрнегін табу үшін (1.20) өрнегін интегралдаймыз.
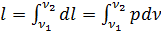 (1.20a)
(1.20a)
Бұл жерде жұмыс күй функциясы емес процесс функциясы, сондықтан dl толық дифференциал емес. Термодинамикалық процесстер есебін жеңілдету үшін m кг масса үшін i - функциясын, ал 1 кг үшін i - функциясын энтальпия деп аталатын функцияны Гиббс енгізді. Энтальпия деп -қарастырып отырған дене көлемінің қысымға көбетіндісінің ішкі энергия қосындысына тең күй функциясын атайды
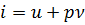 (1.21)
(1.21)
(1.21) теңдеуді дифференциалдап,
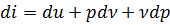 (1.22)
(1.22)
(1.22) теңдеуінен du ішкі энергия өзгерісін анықтап, (1.20) теңдеуін ескере отырып, (1.19)теңдеуіне қойып келесі теңдеуді аламыз
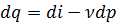 (1.23)
(1.23)
(1.23) теңдеуді интегралдап, төмендегі 1-2 процесстегі жылу мөлшерін анықтауға болады
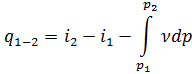
Орныққан жұмыс формуласын қорыту үшін төменде көрсетілген процессті қарастырамыз (сур.6).
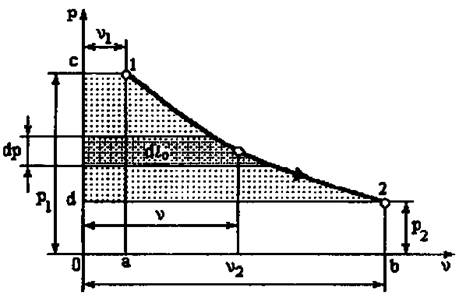
сурет 6. Поршеньдік цилиндрдегі газдың сығылу мен ұлғаю жұмыстарын анықтауға арналған диаграмма
мұндағы c - 1 сызығы двигатель цилиндрін газбен (сұйық) толтыру процесіне сәйкес. Сыртқы ортадан газға жасалынған жұмыс мынаған тең l 1 - p 1 , яғни 0 - c - 1 - a ауданы. Бұл жұмыс оң. 1 - 2 сызығы газдың ұлғаю процесі. Бұл жерде ұлғаю жұмысы атқарылады.
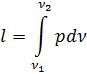
2 - d - cызығы двигатель цилиндрінен газды ығыстыруына сәйкес. Бұл жұмыс теріс, мынаған тең
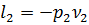
Жоғарыда аталған жұмыстардың алгебралық қосындысы графиктегі c - 1 -2 - d ауданына тең. Бұл аудан машинаға енгізу жұмысы мен газды машинадан шығару жұмысы ескерілетін орналастыру жұмысын (располагаемая) l 0 береді, яғни
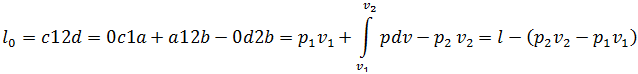
Осыдан
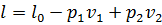 (1.24)
(1.24)
Осы теңдеуді соңғы процесс үшін жазылған Q = ∆ U + L термодинамиканың бірінші заңына қойып, төмендегіні аламыз
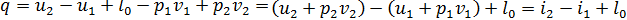
осыдан
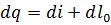 (1.25)
(1.25)
Алынған теңдеу (1.23) теңдеуімен сәйкес келеді. Бұл теңдеу термодинамиканың бірінші заңының математикалық формасы. Егер термодинамикалық процесте P=const болса, онда (1.23) теңдеу төмендегідей түрде жазылады
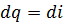
немесе соңғы процесс үшін
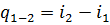
Осылайша энтальпияның физикалық мағынасы, изобаралық процесте энтальпияның өзгерісі жүйенің алған немесе берген жылу мөлшеріне тең.
Қоршаған ортамен жылу алмаспайтын жағдайда (адиабаталық процесте, dq = 0) (1.23) - теңдеу dl 0 = - di немесе l 0 = i 1 - i 2 . Сонымен dq = 0 болғанда пайдалы жұмыс процестің бастапқы және соңғы энтальпиялар айырымна тең. Энталпия тәуелсіз күй параметрлерінің функциясы болғандықтан, оның толық дифференциалы үшін тәуелсіз айнымалыларда v,p; v,T; p,T сәйкесінше төмендегі қатынастар орындалады.
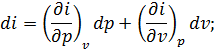
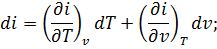
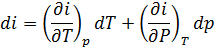
Идеал газдың энтальпиясы ішкі энергия сияқты температураның ғана функциясы болып, молекулалар арасында өзара әсер күші болмағандықтан көлем мен қысымнан тәуелсіз болады.