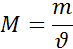
Сан есептерінің оқу-тәрбиелік маңызы және жіктелуі.
Сандық мәліметтер заттар мен құбылыстарды сан жағынан сипаттай отырып,химияны оқытудың білім мен тәрбие беру және оқушылардың ақыл-ойын дамыту міндеттерін нәтижелі жүзеге асыруға жәрдемдеседі.
Сан есептері арқылы жаңа білім беріледі, алынған білім нығайтылады,жетілдіріледі және қолданылады.Заттар мен кұбылыстардың арасындағы сандық қатынастардыашу арқылы пәнаралық байланыс жүзеге асады, оқушыларда ғылымиматериалистік козқарас қалыптасады. Еңбек сүйгіштігі, мақсатынажету жолындағы табандылығы, өз ісіне жауапкершілігі артады. Есеп шығару барысында түсіну, талқылау, ой тұжырымын жасаужәне дәлелдеуге тура келеді.
Есептеулер жасау арқылы химиялық теориялардың,заңдардың және ұғымдардың мәні ашылады. Салыстыру,талдау,жинақтау, жалпыдан жекеге, жекеден жалпыға ауысып,ойлау арқылы оқушылардың ақыл-ойы дамиды,интеллектуалды біліктері мен дағдылары қалыптасады.
Шын мәнісінде есептеулер объектілердің өздері арқылы емес,оларды белгілейтін формула, теңдеу және термин арқылы жүзегеасады.Сан есебінің эр типі бірнеше түрге бөлінеді. Мәселен, формулабойынша есептеулердің түрлері: а) заттың салыстырмалымолекулалық массасын есептеу; ә) заттағы элементтердің массақатынасын табу; б) элементтердің масса үлесін анықтау; в) моль ұғымымен байланысты есептеулер; г) газдардың тығыздығын табу; д) химиялық формула табу есептері және т.б. Теңдеулер жәнеерітінділер бойынша есептеулердің түрлері жеке кластар бойыншақарастырылады.
С.Г.Шаповаленко оқу материалының сипаты, түрі және символикасы бойынша сан есептерін жеті типке бөледі:
Есептерді жіктеуді бір негізге келтіру үшін химияның зерттеу объектілері немесе оларды бейнелейтін химияның тілі тұрғысынан қарауға болады,мысалы:
- Химиялық формулалар бойынша есептеулер
- Химиялық теңдеулер бойынша есептеулер
- Химиялық терминдер арқылы
- Күрделі заттағы элементтердің массалық үлесін оның формуласы бойынша есептеу
- Ерітіндіде еріген заттың массалық үлесін есептеу
- Реакцияға кірісетін заттардың біреуінің белгілі массасы бойынша түзілген заттың массасын есептеу және т.б.
Формула бойынша есептеу түрлері:
Сан есептерін шешу тәсілдері:
Сан есептерін шешу тәсілдері және әдістемесі.
Сан есептерінің екі жағы бар.
Біріншісі - заттармен,химиялық реакциялармен және ұғымдармен юайланысты химиялық мазмұны.
Екіншісі -сандық мәліметтермен жүзеге асырылатын математикалық амалдары.Математикалық мүшелеріне қарай сан есептерін шешу бірге келтіру,пропорция құру,алгебралық,грфикалық және алгоритмдік тәсілдер деп жіктеледі.Есептерді шешудің бір тәсілі ғана (пропорция құру) жиі қолданылады.
Есептеулердің химиялық теңдеулер бойынша енгізілу реті.
|
Тақырыбы: |
Енгізілетін есептің типі |
|
VIII сынып Алғашқы ұғымдар Оттек.Оксидтер.Жану IX сынып Электролиттік диссоциациялау Азот топшасы Көміртек топшасы X сынып Қаныққан көмірсутек |
Химиялық теңдеу бойынша реакцияға кіріскен немесе шыққан заттардың біреуінің белгілі мөлшері бойынша қалғандарныың массасын есептеу Термохимиялық теңдеулер бойынша есептеулер Химиялық теңдеулер бойынша реакцияға түскен немесе шыққан заттардың біреуінің белгілі мөлшері бойынша газдың көлемін табу Реакцияласушы заттардың біреуі артығымен алынғанда химиялық теңдеулер бойынша есептеу Теориялылығын салыстырғандағы өнім шығымының массалық үлесін пайызбен табу. Қосымшасы бар бастапқы заттың берілген массасы немесе көлемі бойынша реакция өнімінің массасын немесе көлемін табу Газ күйіндегі заттың молекулалық формуласын табу(реакция өнімдерібойынша) |
Бір типке немесе түрге жататын есепті әр түрлі тәсілменшығаруға, жоғары сыныптарда оқушылардың математикаданбілімінің өсуіне қарай тәсілді күрделілендіруге және ықшамдауғажете назар аудару керек. Бұл сыныптарда есепті шешудің жинақтапқорытылған жалпы тәсіліне ауысқан тиімді. Есептерді шығаруғабарлық оқушыны бірдей қатыстырып, өзін-өзі бақылауға, өздігіненесептер құрастыруға үйретсе ғана олардың білімі мен білігі тиянақтыболады. Сан есептері барлық сабақтарда, бір сабақтың әр кезеңіндешығарылуы мүмкін. Жаңа сабақты түсіндіруге сан есептері теорияны, заңды, ұғымдынақтылау немесе қорытып шығару үшін пайдаланылады. Мәселен,құрам тұрақтылық заңы темір мен күкірттің әрекеттесуші массаларыарқылы түсіндіріледі, артық алынған массаның реакцияға кіріспейтінінақтылы сандармен дәлелденеді. Масса сақталу заңыныңақиқаттығына есептер шығару арқылы оқушылардың көзін жеткізеді.
VIII сыныпта шығарылатын есептердің типтері.
Химиялық формула бойынша есептеулер.
Заттың салыстырмалы молекулалық массасын есептеу.
1-есеп. Мыс сульфатының салыстырмалы молекулалық массасын есептеңіздер.
Шешуі:
Заттың салыстырмалы молекулалық массасы зат құрамына кіретін атомдардың санына көбейтілген салыстырмалы атомдық массаларының қосындысына тең,ол жалпы түрде былай өрнектеледі:
Mr(зат)=Ar(эл 1 )×n 1 +Ar(эл 2 )×n 2 +Ar(эл 3 )×n 3 +…
Мұндағы :
Mr-салыстырмалы молекулалық масса
Ar-салыстырмалы атомдық масса
Эл- элемент
n-атом саны.Мыс сульфатының химиялық формуласы- CuSO 4
Mr (CuSO 4 )=Ar(Cu)×1+Ar(S)×1+Ar(O)×4
Mr(CuSO 4 )=64×1+32×1+16×4=160
Жауабы : Mr(CuSO 4 )=160
Элементтің масса үлесін табу .
Зат құрамындағы элементтің массалық үлесі бірдің ішіндегі бөлшек санмен немесе пайызбен табылады. Заттағы элементтің масса үлесі элемент атомдарының массасы,молекулалық массасаның қанша бөлігі екенін көрсетеді:
w( эл )=A r ( эл )×n/Mr
2- есеп . Мыс (ІІ) оксидіндегі мыстың және оттегінің массалық үлесін есептеңіздер.
Шешу барысы: а) есептің шартын жазу; ә) заттың формуласын жазу; б) элементтердің салыстырмалы атомдық массаларын тауып, салыстырмалы молекулалық массаны есептеу; в) сан мәндерін формулаға қойып есептеу.
Шешуі :
CuO
W(Cu) -? W(O)(о)-?
Ar(Cu)=64
Ar(O)=16
Mr(CuO)=64+16=80
W(Cu)=Ar(Cu)×1
W(Cu)=64=0,8 немесе 80%
W(O)=16×1/80=0,2 немесе 20%
Жауабы : CuO 80% мыс , 20% оттегі бар
Зат мөлшері ұғымымын пайдаланып жүргізілетін есептеулер .
Моль-негізгі ұғым,одан мольдік масса және мольдік көлем ұғымдары туындайды. Заттың массасын есептеуге арналған
формула:
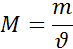
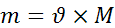
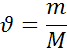
3-есеп. Массасы 4,5г судағы моль санын табыңыздар.
Берілгені:
m(H 2 O)=4.5 г
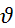 (H
2
O)-?
(H
2
O)-?
M(H 2 O)=Mr(H 2 O)×1 г / моль
M(H 2 O)= 18г/моль
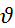 (H
2
O)=4.5 г /18 г/моль= 0,25 моль
(H
2
O)=4.5 г /18 г/моль= 0,25 моль
Химиялық теңдеулер бойынша есептеулер.
Химиялық теңдеулер бойынша есептер шығарғанда химиялық формула,салыстырмалы молекулалық масса,моль,мольдік масса ұғымдары пайдаланылады.
1-есеп.
64,4 г су айырылғанда түзілетін сутегінің массасын есептеңіздер.
Есепті шығару реті:
1) есептің шартымен мұқият танысу;
2)Есептің шартын символика арқылы жазу;
3) Реакция теңдеуін жазу
4)Теңдеу бойынша есепті шығаруға қажетті мәліметтерді анықтау
Есепті бірнеше тәсілмен шығаруға болады.
Есептің шешуі: 1-тәсіл.
Берілгені:
m(H 2 O)=64.8г
2H 2 O=O 2 +2H 2
m(H 2 )=?
M(H 2 O)=18 г/моль
m(H 2 O)=2 моль ×18 г/моль=36 г
M(H 2 )= 2г/моль
m(H 2 )=2 моль×2 г/моль= 4г
Есептің шартында берілген судың массасын теңдеу бойынша табылған массасымен салыстырамыз 64.8г>36г,ол 1,8 есе көп.. Демек, шығатын сутегінің массасы да 1,8 есе көп болуы керек:
4г×1,8=7,2г
Жауабы: 64,8 г судан 7,2 г сутегі бөлінеді
2-тәсіл. Теңдеудегі формулалардың үстіне есептің шартында берілгенін, ал астына теңдеуден табылған шамаларды жазамыз:
64,8 г mг
2H 2 O= O 2 +2H 2
36г 4г
Бұдан 36 г су айырылғанда 4 г сутегі түзілетіні көрінеді, бұл тәуелділікті пропорция түрінде былай жазамыз:
64,8г:36г= mг:4
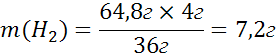
Ерітіндідегі еріген заттың массалық үлесін табу.
1-есеп: 332,5 г суда 17,5 г калий хлориді ерітілген.Ерітіндідегі еріген заттың массасының пайыздық үлесін табыңыздар
Ерітіндідегі еріген заттың массалық үлесі (10) еріген зат массасын ерітіндінің массасына бөлу арқылы табылады:

Берілгені:
m(еріген зат)=17,5г
m(H 2 O)=332,5г
w=?
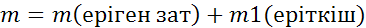
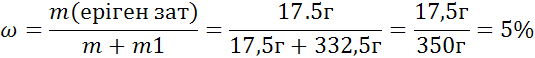
IX СЫНЫПТА ЕНГІЗІЛЕТІН ЕСЕПТЕРДІҢ ТИПТЕРІ.
Әрекеттесуші заттардың біреуі артық алынғанда теңдеу бойынша есептеу 1-есеп. 23,4 натрий хлориді күкірт қышқылымен әрекеттескенде 13,14 г хлорсутек алынды. Хлорсутектің сарамандық шығымын процентпен есептеңдер.
Шешуі :
m(NaCl )= 23,4г
m(HCl)= 13,4г
п.ш.(HCl)=?
Өнімнің процентпен алынған шығымы мына формуламен өрнектеледі:
Демек, теңдеу бойынша хлорсутектің теориялық шығымын есептеу керек.
23,4г xг
2NaCl+H 2 SO 4 = 2HCl+Na 2 SO 4
2×58,5 г/моль 2моль×36,5 г/моль
Бұдан 23,4г: 117г= x:73г
х=23,4г ×73г/117г = 146,6г HCl
п.ш.(HCl)= 13.4г×100%/14,6г =90%
Жауабы: HCl-дың сарамандық шығымы 90%
Х сыныпта енгізілетін есептердің типтері.
Заттардың молекулалық формулаларын табу.
1-есеп. Салыстырмалы молекулалық массасы 46-ға тең бір атомды спирттің молекулалық формуласын табыңыз.
Шешуі:
1. Бір атомды спирттердің жалпы формуласы C n H 2n+1 OH
2. Формуланы түрлендіру арқылы:
C n H 2n+1 OH=46
14n+1+17=46
14n =46-18
14n =28
n =2
3.n-нің сан мәнін жалпы формуладағы орнына қойсақ C n H 2n+1 OH=C 2 H 5 OH шығады. Жауабы: бір атомды спирттің формуласы C 2 H 5 OH
Қорытынды.
Химия пәнін оқып үйренгенде есептер шығарып, жаттығулар орындаудың маңызы өте зор. Есеп шығарып, жаттығулар орындау білімді тексеру ғана емес, сонымен қатар оқушыларды өздігінен ізденуге де дағдыландырады. Оқушылар өз білімдерінің жетіспейтін тұстарын анықтап,онымен жұмыс істеуге, қосымша және арнайы әдебиеттерді пайдалануға үйренеді. Есеп шығару барысында оқушының білімі, зердесі, ойлау қабілеті дамумен қатар, химиялық білімді, заңдарды, құбылыстарды тереңірек түсінуі қалыптасады.
Есеп шығарудың әр түрлі кезеңдерінің өздеріне тән ерекшеліктері бар, соған сай түрліше талаптар қойылады. Ол талаптар оқушылардың жас ерекшеліктері мен білім дәрежесіне тікелей байланысты. Мұғалім мұндай ерекшеліктерді күні бұрын ескеріп, соған сай жұмыс істеуі керек.
Мұғалім есепті сыныпта шығарады, үйге тапсырма ретінде де береді. Бұл талаптарды орындау үшін химиялық есептер мен жаттығуларды тақырыпқа сәйкес алумен қатар, есептер мен жаттығу жұмыстарын орындаудың дұрыс әдістерін пайдаланудың да зор маңызы бар. Есеп шығарғанда және жаттығу жұмыстарын орындағанда оқушылардың математикадан, физикадан және басқа пәндерден алған білімдерін кең түрде пайдалану керек.
Сонымен, химиялық есептер жаңа сарамандық іскерліктер мен дағдыларды қалыптастыру, химиялық ұғымдар мен мағлұматтарды үйрету, білімнің тереңдігі мен баяндылығын тексеру, проблема қою және проблемалық ахуал туғызу, оқушының әртүрлі деңгейдегі шығармашылық қабілетін тәрбиелеу мақсатында беріледі.